15 de agosto de 2025
3 Min Read
As primeiras imagens 3D do implante de embriões humanas revelam novos detalhes do processo
Analisar movimentos de embriões em ambientes de útero pode oferecer pistas para melhorar a taxa de sucesso da fertilização in vitro
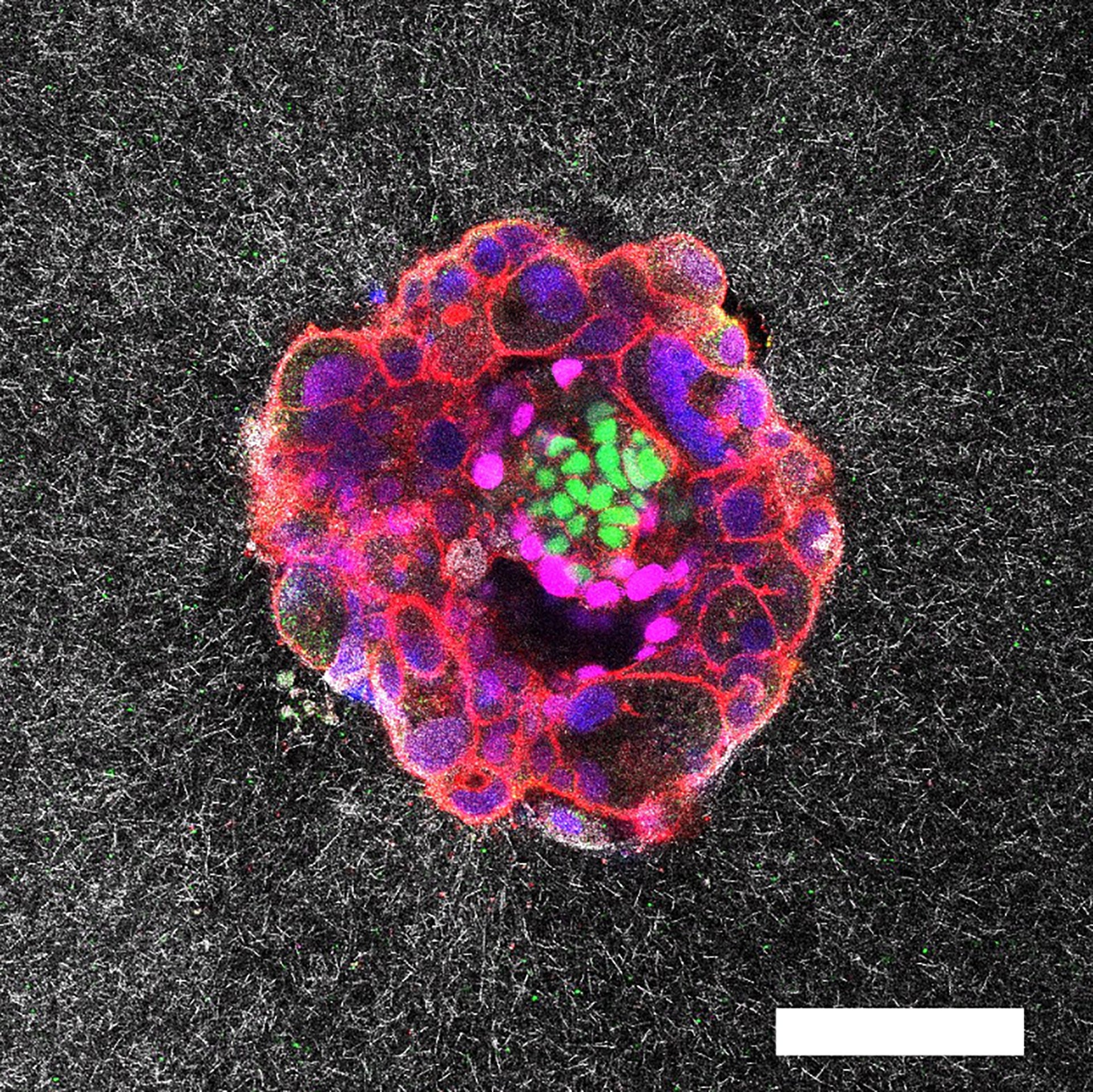
Imagem de microscopia confocal de um embrião humano de nove dias de idade. Proteínas específicas e estruturas celulares foram coloridas na imagem: Oct4 (verde), que está relacionada a células -tronco embrionárias; Gata6 (magenta), que está associado à formação de tecidos precoces; Dapi (azul), que marca o DNA nos núcleos; e faloidina (vermelha), que revela o citoesqueleto de actina. A barra de escala corresponde a 100 µm.
Instituto de Bioengenharia da Catalunha (IBEC)
Os pesquisadores capturaram as primeiras imagens e vídeos tridimensionais em tempo real de um embrião humano implantando em colágeno projetado para imitar o tecido uterino-um estágio-chave na reprodução. As imagens resultantes, que mostram como os embriões empurram e puxam para se ancorar no útero com detalhes vívidos, podem levar a melhorias para técnicas de fertilização in vitro (fertilização in vitro), dizem os cientistas.
“Isso nos permitirá desenvolver tratamentos direcionados especificamente a implantação, que é o maior obstáculo na reprodução humana”, diz Samuel Ojosnegros, bioengenhista do Instituto de Ciência e Tecnologia de Barcelona na Espanha e co-autor do novo estudo, publicado em publicado em Avanços científicos.
Cinco dias depois que um embrião é fertilizado artificialmente, os médicos de fertilidade devem implantá -lo no corpo para que ele possa continuar a crescer. “O que acontece entre a transferência e o primeiro ultrassom semanas depois é uma caixa preta”, diz Ojosnegros, que também é co-fundador da empresa de biotecnologia Serabiotics. A falha do implante é uma das principais causas de infertilidade – até 60 % dos abortos ocorrem durante esse processo.
Sobre apoiar o jornalismo científico
Se você está gostando deste artigo, considere apoiar nosso jornalismo premiado por assinando. Ao comprar uma assinatura, você está ajudando a garantir o futuro das histórias impactantes sobre as descobertas e idéias que moldam nosso mundo hoje.
A primeira cultura bem -sucedida de embriões humanos além da implantação foi demonstrada em uma placa de Petri em um laboratório em 2016, mas Ojosnegros e sua equipe queriam ver como seria esse processo no tecido 3D que era mais parecido com o do útero.
Para fazer isso, a equipe projetou um sistema ex vivo especial feito de gel e colágeno – uma proteína encontrada no revestimento uterino – e usou embriões doados por pessoas que haviam concluído um processo de reprodução assistida. O sistema funciona, diz Ojosnegros, porque a rede de fibras de colágeno sinaliza para o embrião em um nível molecular de que essa é uma matriz natural.
Ao usar microscópios 3D avançados, os pesquisadores registraram a ação ao longo do tempo. O rastreamento de pequenos movimentos nas fibras do gel lhes permitiu mapear exatamente onde e quão fortemente os embriões estavam puxando. Os pesquisadores fizeram o mesmo com embriões de rato para comparar padrões de movimento.
As filmagens mostraram que os embriões humanos geram uma rede de pequenas forças de tração que ondulam pelo útero. Eles se escondem no tecido circundante de um lado, criando vários pequenos pontos de tração que puxam o revestimento em todas as direções. Os embriões de mouse, por outro lado, se espalham mais pela superfície e puxam principalmente duas ou três linhas fortes.

Embrião compactando e invadindo o tecido uterino.
Quando os pesquisadores aplicaram a tensão externa à matriz, puxando -a com minúsculas pinças, eles notaram os embriões reorientados em relação a essas áreas. Os cientistas sugerem que as micro contrações podem estar orientando o embrião a implantar na direção ideal no útero. “Acreditamos que essas micro contrações são o que o embrião usa para se guiar em direção aos vasos sanguíneos e aos nutrientes de que precisa”, explica Ojosnegros, acrescentando que são necessários mais estudos para confirmar essa hipótese.
Nos experimentos de camundongo e humano, a força e o padrão dessas forças estavam ligados à saúde do embrião, o que significa que os embriões que puxavam menos tinham menos probabilidade de invadir com sucesso o tecido. Observar a implantação em tempo real em um modelo 3D é um “salto quântico” em comparação com as observações bidimensionais que já existem, diz o biólogo do desenvolvimento Claudia Spits da Universidade Livre de Bruxelas, que não estava envolvida na pesquisa. Manter um embrião vivo nessas condições é extremamente difícil, diz ela. “O que você vê em um vídeo de 10 segundos são anos definindo essas (condições) para que o embrião possa sobreviver”, acrescenta Sta.

Dois embriões implantando no útero.
“Este estudo prepara o cenário para explorar a dinâmica da implantação em detalhes sem precedentes”, diz Magdalena & Zdot; Ernicka-Goetz, bióloga do desenvolvimento do Instituto de Tecnologia da Califórnia, que não esteve envolvido na pesquisa. As descobertas contribuem para o crescente corpo de trabalho sobre observações pós -implantação humanas publicadas nos últimos nove anos, diz ela, e “esses estudos são um passo emocionante para entender um estágio de desenvolvimento humano que há muito tempo está escondido da vista”. Notas futuras de pesquisas, & Zdot; Ernicka-Goetz, ainda é necessária para comparar como os embriões se comportam em diferentes plataformas “semelhantes a útero” para ver se as trajetórias de desenvolvimento diferem.
A matriz desenvolvida pela equipe de Ojosnegros não se destina a procedimentos de fertilização in vitro, mas pode ser uma ferramenta valiosa para empresas farmacêuticas e laboratórios testando soros ou diferentes tipos de embriões. “Ao começar a entender como o embrião se comporta”, diz Ojosnegros, “podemos começar a pensar na possibilidade futura de selecionar embriões saudáveis ou mais capazes de implantar”. Spits permanece cético em relação a essa afirmação, porque a replicação dessa tecnologia em outros laboratórios pode ser um grande desafio. Mas ela diz que os resultados são um “grande passo adiante” na tecnologia que pode ter aplicativos futuros assim que outros laboratórios podem fazer seus próprios implantes em 3D.